ESTUDO FÍSICO DOS GASES
Veja aqui a teoria dos gases e uma lista de exercícios para resolver.

Nesse post vamos trazer uma explicação detalhada do estudo físico dos gases e no final veja uma lista de exercícios com gabarito. A expressão estado de um gás designa a situação em que esse gás se encontra, ou seja, como ele “está”. Especificar o estado de um gás significa dizer qual é o valor de:
- Pressão ( P )
- Temperatura ( T )
- Volume ( V )
dizemos que P, T e V são variáveis de estado.
Estudo Físico dos gases
UNIDADES DE VOLUME
1cm3 = 1ml 1dm3 = 1 l 1m3 = 103l
UNIDADES DE PRESSÃO
1atm = 760mnHg 1atm = 760Torr
UNIDADES DE TEMPERATURA
K = Co + 273
– PRESSÃO DE UM GÁS é a manifestação da colisão de suas moléculas contra a parede do recipiente.
Estudo Físico dos gases
LEIS FÍSICAS DOS GASES
- Lei de Boyle-Mariotte : “A temperatura constante , o volume ocupado por determinada massa gasosa é inversamente proporcional a sua pressão ( Estudo Físico dos gases )
ISOTÉRMICA – P1V1 = P2V2
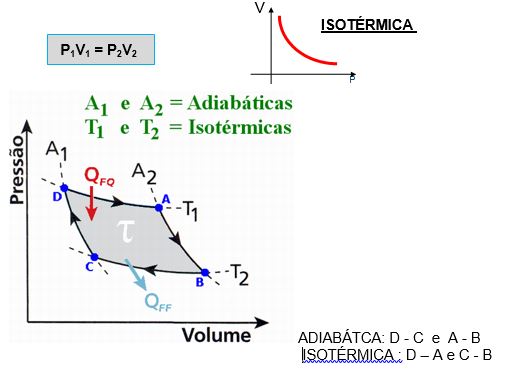
ISOBÁRICA
V1 / T1 = V2 / T2
Lei de Gay-Lussac : “A pressão constante , o volume ocupado por determinada massa gasosa é diretamente proporcional a sua temperatura absoluta”. ( Estudo Físico dos gases )
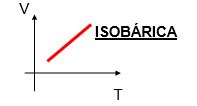
ISOVOLUMÉTRICA
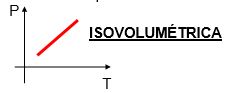
- Lei de Charles : “A volume constante , a pressão exercida por uma determinada massa gasosa é diretamente proporcional a sua temperatura absoluta”. ( Estudo Físico dos gases )
P1 / T1 = P2 /T2
Condições normais de temperatura e pressão (CNTP):
T = 0oC ou 273K
V = 22,4 L
P = 1 atmosfera (1 atm)
GÁS PERFEITO (IDEAL)
O gás perfeito obedece, rigorosamente, as leis e fórmulas estudadas neste capítulo. Porém a PRESSÃO MUITO ALTA ou TEMPERATURA MUITO BAIXA o GÁS REAL sempre se afasta do comportamento de um gás perfeito. Então podemos dizer que quanto mais rarefeito ele estiver mais perfeito será.
Equação Geral dos Gases
Equação de Estado dos Gases Perfeitos
Nas CNTP temos:
P.V/n.T = 1 . 22,4/273 = 0,082 atm.L/K.mol
logo R = P.V/nT para 1 mol
R = 0,082 atm.L/k.mol
Então com a constante R chegamos na equação geral dos gases:
P.V = n. R.T
Fenômeno de Difusão
DIFUSÃO – Fenômeno através do qual os gases se misturam de forma rápida e homogênea, formando um sistema monofásico. Quando ocorre sua saída para a atmosfera, eles se espalham, vale dizer, se difundem
A TEORIA CINÉTICA DOS GASES
O modelo utilizado para descrever o estado gasoso é a Teoria Cinética dos Gases. Esta teoria baseia-se nos seguintes postulados
- As unidades elementares encontram-se em rápido e constante movimento em linha reta;
- As distâncias entre elas são muito grandes em relação ao seu tamanho;
- Pode ser desprezado a interação entre as unidades elementares;
- Quando ocorrem colisões entre as unidades elementares, a energia é conservada;
- A temperatura é uma medida da energia cinética média das unidades elementares
Veja aqui também:
Nomenclatura de Compostos Inorgânicos
Curso Online de Matemática, Química, Física, Português, Biologia, Redação, Filosofia e Sociologia para o ENEM!

( Estudo Físico dos gases )
Exercícios e para o Enem
01) Qual o volume ocupado por 32g de dióxido de enxofre (SO2) a 127oC e pressão de 2atm ?
a) 4,0 l
b) 6,4 l
c) 7,3 l
d) 8,2 l
e) 9,0 l
02) Um certo gás inicialmente em repouso a 27oC é aquecido sob pressão constante, até que seu volume final seja o triplo do volume inicial. Qual a temperatura final do gás?
a) 600K
b) 700K
c) 800K
d) 900K
e) 1000K
03) Um gás está em um recipiente provido de uma válvula. Abre-se a válvula e permite-se que um décimo do no de mols do gás contido no recipiente escape para o exterior. Supondo que a temperatura inicial do gás seja igual a 0oC, a que temperatura devemos aquecer o gás para que a pressão permaneça inalterada ?
a) 103,3K
b) 203,3K
c) 303,3K
d) 403,3K
e) 503,3K
04) Comprime-se um gás mantendo-se constante a sua temperatura de modo que seu volume se reduza a um terço do valor inicial nessas condições, a pressão do gás sofre um acréscimo de 900mmHg. Qual a pressão inicialmente exercida pelo gás ?
a) 450mmHg
b) 500mmHg
c) 550mmHg
d) 600mmHg
e) 650mmHg
05) A que temperatura deve ser aquecido um frasco aberto para que um quinto do gás que ele encerra a 7oC se escape ?
a) 67oC
b) 77oC
c) 87oC
d) 97oC
e) 107oC
06) A que pressão deve ser submetido 1 litro de gás medido a 1atm e -20oC, para ser comprimido a 1/2 litro quando a temperatura for 40oC ?
a) 1,07
b) 1,27
c) 2,27
d) 2,47
e) 3,07
07) ( Considere todos os recipientes com volumes iguais a “v” e tendo no recipiente 1(P = 6atm); no 2 (P = 2,5 atm) e no 3 vácuo. Ao abrirmos as torneiras, qual a pressão final nos 3 vasos se mantivermos a temperatura constante?
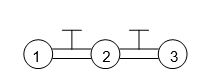
a) 2,43
b) 2,83
c) 3,03
d) 3,23
e) 3,83
08) De acordo a lei de Robert Boyle (1660), para proporcionar um aumento na pressão de uma determinada amostra gasosa numa transformação isotérmica, é necessário:
a) aumentar seu volume
b) diminuir a sua massa
c) aumentar a sua temperatura
d) diminuir o seu volume
e) aumentar a sua massa
09) (UFRGS)- A equação PV = nRT
a) é usada universalmente para todos os gases em qualquer situação
b) só vale para gases ideais nas CNTP
c) pode ser usada para alguns gases reais, mas só nas CNTP
d) é usada com boa aproximação para gases reais principalmente para aqueles mais semelhantes ao modelo ideal
e) descreve situações de gases ideais que em nada se assemelham aos gases reais, dois são modelos teóricos afastados da realidade.
10) Um extintor de incêndio contêm 4,4kg de CO2. O volume máximo de gás liberado na atmosfera a 27oC e 1atm, é, em litros :
a) 0,229
b) 2,64
c) 24,6
d) 229,4
e) 2.460
GABARITO
| 1) d | 3) c | 5) b | 7) b | 9) d |
| 2) d | 4) a | 6) d | 8) d | 10) e |










